〇解剖
1. 机に70%エタノールを噴霧し、アルミホイルを貼り付ける。
2. 滅菌シャーレ(イナ・オプティカ, I-90) 3-5枚にPBSを入れておく
3. テルモシリンジ注射針付(Terumo, SS-01T2613S)にヘパリンNa注5000U/5ml (持田製薬)を吸わせて戻し、デッドスペースに液を満たすようにする。
4. 麻酔薬を29Gマイジェクター(Terumo)で吸引しておく。
5. 体重、臓器重量、操作を記載する用紙を用意する。
6. 臓器、血液、尻尾を保存する1.5mlチューブを用意する。
7. 臓器を固定するScintillation vial (Iwaki)を用意する。
8. 液体窒素、氷、10%-中性緩衝ホルムアルデヒド液(nacalai, 37152-51)を用意する。
9. Balance dish L (イナ・オプティカ, 208008)を電子天秤に乗せ、電子天秤が安定している事を確認する。
10. 動物実験施設に行き、マウスの体重を測定し、かごに入れて持ち帰り、飼育表から削除する。
11. 麻酔薬を10ul/gBW腹腔内注射し、動かなくなるまで待つ。
12. コンフォートサービスタオルの上にマウスを乗せ、70%エタノールを腹部に噴霧し、胸骨下端と外陰部の中間あたりに切れ込みを入れ、手でつまんで上下に皮膚をはがす(切れ込みが下過ぎると、腹部皮下脂肪が上下に裂けて採取し辛くなる)。
13. 腹部中央の腹膜に切れ込みを入れ、斜め上に腹膜を切開する。
14. 肝臓を上にめくって下大静脈近位を露出させ、ピンセットを置いて肝臓をめくった状態に固定する。
15. ヘパリン入りシリンジで下大静脈から採血し、on iceにしておく。
16. 臓器を採取し、PBSで洗い、Balance
dishに乗せて重量を測定し、1.5mlチューブに入れ、液体窒素に浸ける。採取する順番の目安は、肝臓(死後glycogenが急速に消費される)→
その他の腹腔内臓器、皮下脂肪組織(時間が経つと乾燥する)→骨格筋、褐色脂肪組織等。
17. 血液を3000g, 4℃, 10min遠心し、上清を回収する。
18. 血漿、臓器を-80℃で保存する。
臓器の採取方法
腹腔内臓器:乾燥しないよう、適宜PBSで濡らしたキムワイプで湿らせる。
肝臓
1. 横隔膜との連絡を切る
2. 胃との連絡を切る
3. 肝門部を切る
4. 単離した後、胆のうを切除する。
5. 右葉の一部をサンプル用に切除する。
精巣周囲脂肪
1. 一部をサンプル用に切除する。
2. 精巣上体、精管、精巣との連絡を切り、全体を取り出して重量を測定する。
腸間膜脂肪
1. 腸管との連絡を切る
2. 単離した後、一部をサンプル用に切除する。
腎臓
1. 周りの組織ごと大きく単離する
2. 脂肪組織や結合組織を剥離する
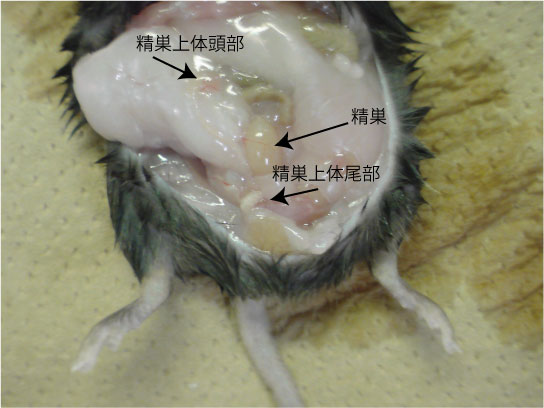
精巣上体尾部:IVF等に使用
1. 精巣上体尾部を確認し、周りの組織ごと切り取る
2. 余分な組織を除去する
腹部皮下脂肪
1. 腹部皮膚との連絡を切る
2. 腹膜との連絡を切る
3. 一部をサンプル用に切除する
4. 残りを取り出して重量を測定する。
ヒフク筋、ヒラメ筋
1. 足首の皮膚に一周切れ込みを入れ、ピンセットでつまんで皮膚を膝まで剥離する。
2. アキレス腱の下にハサミを入れ、膝までスライドさせて筋肉を浮かせる。
3. 踵を切断し、アキレス腱を保持して膝まで剥離し、切断する。
4. 余分な組織を除く。
胸腺
1. 胸膜や心臓との連絡を切る
脳
1. 頭部の皮膚を剥離する
2. 泉門からハサミを入れ、頭蓋骨を除去する
3. 脳の底にハサミを入れ、壊さないようにそっと摘出する
